Dogmat Anfinsena, znany też jako hipoteza termodynamiczna fałdowania białek, jest hipotezą w biologii molekularnej zaproponowaną przez Christiana Anfinsena. Zasadniczo stwierdza ona, że białko wchodzące w swoją pierwotną strukturę — innymi słowy, posiadające określoną sekwencję aminokwasów — ma zakodowaną w tej sekwencji informację wystarczającą do przyjęcia swojej natywnej, trójwymiarowej struktury. Innymi słowy: to sekwencję aminokwasów decyduje w dużej mierze o ostatecznym kształcie białka. W praktyce zasada ta dotyczy wielu, zwłaszcza małych i pojedynczych domenowych białek, podczas gdy dla innych białek potrzebne są dodatkowe czynniki pomocnicze (przyzwoitki — poprawnie: chaperony, czyli białka opiekuńcze).
Dowód i znaczenie historyczne
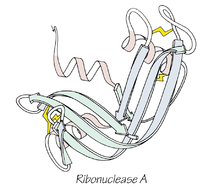
Anfinsen otrzymał w 1972 r. Nagrodę Nobla w dziedzinie chemii za serię eksperymentów na strukturze enzymu rybonukleazy A. Pokazał on, że po całkowitym denaturowaniu tego enzymu (rozłożeniu wiązań niekowalencyjnych i rozbiciu mostków disiarczkowych) i następnie przywróceniu warunków sprzyjających, białko może spontanicznie odzyskać swoją aktywną, natywną konformację. Wyniki te sugerowały, że informacja potrzebna do utworzenia natywnej struktury jest zakodowana w sekwencji aminokwasowej, a nie wymaga zewnętrznej „instrukcji”.
Trzy warunki dogmatu
Dogmat Anfinsena jest często formułowany przez trzy powiązane założenia dotyczące natywnej struktury białka:
- Wyjątkowość — natywna konformacja jest jedyną (lub przeważającą) strukturą o najniższej wartości energii swobodnej dla danej sekwencji; sekwencja nie powinna mieć innej konkurencyjnej konfiguracji o porównywalnej energii.
- Stabilność — niewielkie zmiany warunków (temperatura, pH, stężenie soli itp.) nie powinny powodować łatwej utraty natywnej konformacji; natywna struktura jest termodynamicznie preferowana.
- Dostępność kinetyczna — białko powinno być w stanie osiągnąć natywną konformację w rozsądnym czasie bez konieczności przechodzenia przez niezwykle rzadkie i skomplikowane przejścia (np. tworzenie węzłów, długich poszukiwań konformacyjnych).
Jak białko znajduje swój kształt — fałdowanie białka
Sposób, w jaki cząsteczka białka osiąga natywną strukturę, jest przedmiotem dziedziny fałdowania białka. Początkowo problem ten wydawał się paradoksalny — Paradoks Levinthala pokazuje, że liczba możliwych konformacji jest astronomicznie duża, więc „losowe” przeszukiwanie wszystkich stanów nie mogłoby doprowadzić do natywnej struktury w rozsądnym czasie (dla małego białka już liczby rzędu 10^26 sekund). Rozwiązaniem jest model krajobrazu energetycznego lub „leja energii” — białko porusza się po skomplikowanym, ale uporządkowanym krajobrazie energetycznym, w którym istnieją liczne lokalne dróg prowadzące w dół do globalnego minimum (natwynego stanu), co czyni proces kinetycznie wykonalnym.
W praktyce wiele białek fałduje się ko-translacyjnie (podczas syntezy na rybosomie), a procesy pomocnicze, takie jak formowanie mostków disiarczkowych czy izomeraza disiarczków, wpływają na poprawne ułożenie. Dla większych lub złożonych białek kluczową rolę pełnią chaperony — białka opiekuńcze (np. systemy Hsp70, chaperoniny typu GroEL/GroES), które zapobiegają agregacji i ułatwiają osiągnięcie prawidłowej konformacji.
Wyjątki i ograniczenia
Dogmat Anfinsena obowiązuje w określonych warunkach i dla wielu białek, ale nie jest uniwersalny. Priony są klasycznym wyjątkiem — to białka, które mogą występować w alternatywnych, niezwykle stabilnych konformacjach różniących się od formy natywnej. Zmieniona konformacja priona może katalizować przekształcenie kolejnych cząsteczek tego samego białka do patologicznego kształtu, co prowadzi do agregacji i choroby. W przypadku gąbczastej encefalopatiibydła (Mad Cow Disease), konwersja natywnego białka do formy prionowej prowadzi do śmiertelnych nagromadzeń włóknistych agregatów amyloidowych. Inne choroby związane z tworzeniem się amyloidu, w tym choroba Alzheimera i choroba Parkinsona, również ilustrują sytuacje, w których białka przyjmują patologiczne, stabilne konformacje będące wyjątkiem od prostego odczytu informacji z sekwencji.
Podsumowanie
Dogmat Anfinsena pozostaje fundamentem zrozumienia relacji między sekwencją aminokwasów a strukturą białka: dla wielu białek informacja niezbędna do przyjęcia natywnej konformacji jest zawarta w sekwencji. Jednak mechanizmy fałdowania są złożone, obejmują aspekt kinetyczny i wpływ środowiska komórkowego, a dla licznych białek niezbędne są czynniki pomocnicze lub istnieją patologiczne alternatywne struktury (priony, amyloidy), które stanowią istotne wyjątki od tej hipotezy.