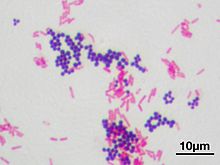
Barwienie metodą Grama (lub metodą Grama) jest podstawową techniką mikroskopową służącą klasyfikacji bakterii na dwie duże grupy: gram-dodatnie i gram-ujemne. Nazwa pochodzi od nazwiska jej wynalazcy, Hansa Christiana Grama.
Przebieg techniki — krok po kroku
Typowy schemat barwienia Grama obejmuje następujące etapy:
- Utrwalenie preparatu (zwykle ogrzewanie nad palnikiem lub utrwalenie metanolem),
- Nałożenie barwnika podstawowego — fiolet krystaliczny,
- Dodanie jodu (mordantu), który tworzy kompleks fiolet krystaliczny–jod (CV–I),
- Spłukanie i dekoloryzacja (odbarwianie) za pomocą alkoholu lub mieszaniny acetonu i etanolu — etap krytyczny,
- Nałożenie barwnika kontrastowego — zwykle safraniny lub fuksyny,
- Oglądanie preparatu w mikroskopie świetlnym przy olejku imersyjnym.
Mechanizm barwienia
Metoda Grama barwi bakterie zgodnie z chemicznymi i fizycznymi właściwościami ich ścian komórkowych. Mechanizm można opisać krótko tak:
- U bakterii Gram-dodatnich gruba warstwa peptydoglikanu zatrzymuje kompleks CV–I i po dekoloryzacji komórki pozostają fioletowe (nie tracą barwnika podstawowego).
- U bakterii Gram-ujemnych cienka warstwa peptydoglikanu oraz zewnętrzna błona lipidowa (zawierająca lipopolisacharyd, LPS) ulegają częściowej ekstrakcji/depolaryzacji podczas dekoloryzacji, dzięki czemu kompleks CV–I jest usuwany i komórki przyjmują późniejszy barwnik kontrastowy (czerwony/różowy).
Wynik i interpretacja
- Gram-dodatnie: komórki barwią się na kolor fioletowy/granatowy (połączenie fioletu krystalicznego i jodu).
- Gram-ujemne: komórki stają się różowe/czerwone po zastosowaniu safraniny lub fuksyny jako barwnika kontrastowego.
Wynik barwienia dostarcza szybkiej informacji o budowie ściany komórkowej i pomaga wstępnie ukierunkować identyfikację drobnoustroju oraz wybór antybiotykoterapii.
Ograniczenia i przyczyny błędów
Nie wszystkie bakterie można jednoznacznie sklasyfikować metodą Grama. Do głównych ograniczeń należą:
- Stan hodowli: stare kultury mogą ulegać autolizie i dawać wynik „gram-ujemny” mimo że gatunek jest gram-dodatni.
- Nieprawidłowe odbarwianie: zbyt długie odbarwianie może spowodować fałszywie gram-ujemny rezultat; zbyt krótkie — fałszywie gram-dodatni.
- Bakterie o nietypowej ścianie: np. Mycobacterium (ściana bogata w lipidy/wosk — wymagają barwienia ziehl-neelsena, czyli techniki kwasooporne), Mycoplasma (brak ściany komórkowej — barwienie Gramem nie jest przydatne).
- Organizmy gram-zmienne lub gram-nieokreślone: niektóre gatunki dają mieszane lub trudne do interpretacji obrazy.
- Wpływ zewnętrzny: złe utrwalenie, grubość preparatu, obecność biofilmu lub materiału organicznego może zaburzać wynik.
Przykłady i wyjątki
Typowe przykłady:
- Gram-dodatnie: Staphylococcus, Streptococcus, Bacillus, Clostridium.
- Gram-ujemne: Escherichia, Salmonella, Pseudomonas, Neisseria.
Istnieją też organizmy, których wynik barwienia nie odpowiada w pełni ich filogenetycznemu pokrewieństwu — stąd Gram jest testem morfologiczno-chemicznym, nie pełną metodą taksonomiczną.
Zastosowanie kliniczne i laboratoryjne
- Barwienie Grama jest zwykle pierwszym krokiem w diagnostyce bakteryjnej — szybkie informacje o rodzaju bakterii pomagają w wyborze wstępnego leczenia (np. antybiotyki skierowane na bakterie gram-dodatnie lub gram-ujemne).
- Pomaga także w ocenie preparatów z płynów ustrojowych (np. plwocina, płyn mózgowo-rdzeniowy, krew) oraz w kontroli jakości hodowli i badań mikrobiologicznych.
- W laboratorium mikrobiologicznym wynik barwienia Grama kieruje dalszymi testami identyfikacyjnymi i dojrzewaniem procedury diagnostycznej.
Krótka historia
Gram opracował tę technikę we współpracy z innym naukowcem, Carlem Friedländerem, w szpitalu w Berlinie. Jednak Gram najpierw użył testu, aby ułatwić dostrzeżenie bakterii w płucach. Swoją gotową metodę opublikował w 1884 roku. Od tego czasu barwienie Grama stało się fundamentalnym narzędziem w mikrobiologii klinicznej i badaniach podstawowych.
Wskazówka praktyczna: dla uzyskania wiarygodnych wyników używa się świeżych kultur (zwykle 18–24 godziny) oraz kontrolnych szczepów referencyjnych; interpretację zawsze należy łączyć z danymi klinicznymi i dalszymi badaniami identyfikacyjnymi.