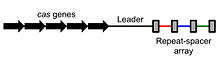
CRISPR to termin używany w mikrobiologii. Jest to skrót od Clustered Regularly-Interspaced Short Palindromic Repeats. Są to naturalne segmenty kodu genetycznego występujące u prokariotów: posiada je większość bakterii i archaidów. Sekwencje CRISPR składają się z powtarzających się krótkich sekwencji rozdzielonych tzw. spacerami — fragmentami DNA pochodzącymi z wirusów lub plazmidów, które dane komórki kiedyś napotkały.
Funkcja naturalna — adaptacyjny system odpornościowy
CRISPR jest częścią adaptacyjnego systemu odpornościowego prokariotów. Działa wieloetapowo:
- Adaptacja (zapamiętywanie) — po infekcji bakteria może włączyć fragment patogenu jako nowy spacer w obrębie loci CRISPR.
- Ekspresja — z CRISPR transkrybowane są krótkie RNA (crRNA), które zawierają sekwencje spacerów rozpoznające obce DNA/RNA.
- Interferencja — crRNA w kompleksie z białkami typu Cas (CRISPR-associated) prowadzi do rozpoznania i przecięcia DNA lub RNA intruza, unieszkodliwiając go.
System ten pozwala prokariotom „zapamiętywać” i skutecznie zwalczać bakteriofagi i mobilne elementy genetyczne, takie jak plazmidy.
Główne składniki systemu CRISPR
- Powtórzenia i spacery — powtarzające się sekwencje i unikatowe spacery pochodzące od patogenów.
- Białka Cas — enzymy odpowiedzialne za cięcie kwasu nukleinowego; najpopularniejszym przykładem w biologii molekularnej jest Cas9, ale istnieją też Cas12, Cas13 i inne o różnych właściwościach.
- crRNA i tracrRNA / sgRNA — RNA prowadzące; w systemach inżynieryjnych często używa się zsyntetyzowanego pojedynczego RNA (sgRNA), łączącego funkcje tracrRNA i crRNA.
- PAM (protospacer adjacent motif) — krótka sekwencja w docelowym DNA, wymagana przez niektóre białka Cas (np. Cas9) do rozpoznania i cięcia.
Mechanizm działania w inżynierii genetycznej
W zastosowaniach laboratoryjnych najczęściej wykorzystuje się warianty białka Cas (np. SpyCas9) zaprogramowane przez odpowiednie guide RNA (sgRNA). Mechanizm skróconymi krokami:
- sgRNA wiąże się z białkiem Cas i kieruje kompleks do krótkiej, komplementarnej sekwencji w genomie.
- Po związaniu, jeśli obecny jest odpowiedni PAM, Cas wykonuje cięcie DNA — zwykle dwuniciowe pęknięcie.
- Komórka naprawia pęknięcie za pomocą mechanizmów naprawy: NHEJ (niereprezycyjna naprawa) może prowadzić do insercji/delecji (indeli) i utraty funkcji genu; HDR (homologiczna rekombinacja) umożliwia wstawienie zaprojektowanej sekwencji, jeśli podany jest szablon.
Zastosowania
Systemy CRISPR-Cas zrewolucjonizowały biologię molekularną i mają szerokie zastosowania:
- Edycja genów — wyciszanie genów (knockout), wprowadzanie lub naprawa mutacji, wstawianie sekwencji.
- Biotechnologia i rolnictwo — tworzenie odmian roślin odpornych na choroby, zwiększanie plonów, skracanie czasu hodowli.
- Medycyna — terapie genowe (np. korekta mutacji powodujących choroby monogenowe), potencjalne terapie przeciwnowotworowe, immunoterapia.
- Diagnostyka — techniki oparte na Cas12/Cas13 (np. DETECTR, SHERLOCK) do szybkiego wykrywania patogenów, w tym wirusów.
- Modyfikacje funkcjonalne — edytory zasad (base editors) i prime editing pozwalają na precyzyjne zmiany pojedynczych nukleotydów bez wprowadzania dwuniciowych pęknięć.
- Badania podstawowe — szybkie tworzenie linii komórkowych i zwierzęcych z określonymi modyfikacjami w celu badania funkcji genów.
- Gene drives — strategie mające na celu rozprzestrzenianie określonych genów w populacjach dzikich organizmów (potencjalne zastosowanie w kontroli owadów przenoszących choroby).
Ograniczenia, ryzyka i aspekty etyczne
Pomimo ogromnego potencjału, stosowanie CRISPR wiąże się z wyzwaniami:
- Efekty pozamierzone (off-target) — cięcia w niezamierzonych miejscach genomu mogą prowadzić do mutacji i konsekwencji biologicznych.
- Dostarczenie do komórek — skuteczna i bezpieczna metoda wprowadzenia systemu CRISPR do tkanek (wektor wirusowy, nanocząsteczki) pozostaje trudna zwłaszcza in vivo.
- Odpowiedź immunologiczna — u ludzi białka Cas pochodzące z bakterii mogą być rozpoznawane przez układ odpornościowy.
- Ryzyko ekologiczne — zwłaszcza w przypadku gene drive; niezamierzone skutki dla ekosystemów mogą być trudne do odwrócenia.
- Aspekty etyczne — edycja zarodkowa i modyfikacje linii germinalnej budzą poważne kontrowersje i są regulowane w wielu jurysdykcjach.
Przyszłość
Badania nad CRISPR stale postępują. Rozwój nowych wariantów enzymów Cas, udoskonalenie metod dostarczania, zwiększenie precyzji (mniejsze off-target), a także powstanie kolejnych narzędzi diagnostycznych i terapeutycznych sprawiają, że CRISPR pozostaje jedną z najbardziej obiecujących technologii biologii współczesnej. Jednocześnie rośnie znaczenie odpowiedzialnych regulacji i debaty publicznej, aby korzyści były osiągane bez nieakceptowalnego ryzyka.
Mają one potencjał do modyfikowania genów niemal każdego organizmu. Są częścią narzędzia, które umożliwia precyzyjnie ukierunkowane wycinanie i wstawianie genów w modyfikacjach genetycznych (GMO). Trwają prace nad znalezieniem sposobu ich wykorzystania do zwalczania chorób wirusowych u ludzi oraz do innych zastosowań medycznych i przemysłowych.