Zasada Niepewności, często nazywana również zasadą Niepewności Heisenberga, opisuje fundamentalne ograniczenie w tym, jak dokładnie można jednocześnie znać pewne pary wielkości fizycznych, z których najbardziej znaną parą są pozycja i pęd. To nie jest jedynie ograniczenie techniczne przyrządów pomiarowych, lecz cecha samej natury mikroskopowego świata.
Czym jest zasada niepewności?
Werner Heisenberg natknął się na to ograniczenie, analizując sposób, w jaki pomiar jednej wielkości wpływa na drugą. W uproszczeniu: im dokładniej określimy pozycję cząstki (Δx mała), tym większa staje się niepewność jej pędu (Δp duża), i odwrotnie. W zapisie matematycznym najczęściej spotykanym w literaturze występuje nierówność
Δx · Δp ≥ ħ/2,
gdzie ħ (czyt. „h kreskowane”) to stała Plancka podzielona przez 2π. Ta formuła określa minimalny możliwy iloczyn niepewności pozycji i pędu dla dowolnego stanu kwantowego.
Intuicja i przykłady
W świecie makroskopowym, jak podczas obserwacji samochodu na drodze, nie odczuwamy tej zasady — niepewności są tak małe, że je pomijamy. Możemy zmierzyć pozycję samochodu i potem jego prędkość z taką dokładnością, że nadal traktujemy jego ruch jako dobrze określoną trajektorię. Jednak w skali atomowej sprawy wyglądają inaczej.
Wyobraźmy sobie obserwację elektronu. Jeśli bardzo dokładnie zlokalizujemy jego pozycję, to zgodnie z zasadą niepewności zwiększymy niepewność jego pędu — a więc jego przyszła trajektoria stanie się „rozmyta”. Ten efekt nie wynika tylko z zakłócenia spowodowanego aparaturą, ale z faktu, że cząstka w stanie kwantowym nie ma jednocześnie ostro określonej pozycji i pędu.
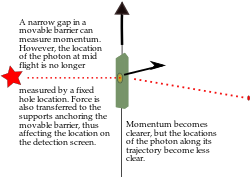
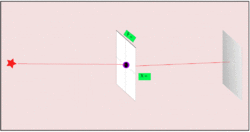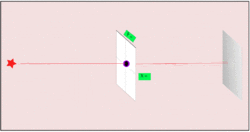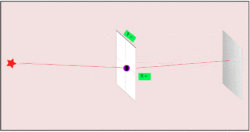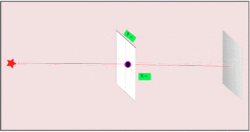
Analogie używane w literaturze pomagają to zilustrować: jeśli mierzymy elektrony lecące na ekran detekcyjny trafi i próbujemy je dokładnie zlokalizować po drodze, obserwujemy, że dokładniejsza lokalizacja powoduje zwiększenie rozrzutu trafień na ekranie. Gdy natomiast mierzymy elektrony tak, by ustalić ich trajektorię, stają się mniej określone w położeniu docelowym — ustalenie lokalizacji czyni trajektorię bardziej niepewną.
Podobnie, gdybyśmy zamiast piłek baseballowych, rzucali elektronami i umieścili aparaturę rejestrującą „gdzie jest cząstka w połowie lotu”, włączenie kamer mogłoby zmienić obserwowany rozrzut trajektorii. Im dokładniej chcemy wiedzieć, gdzie była cząstka w danym momencie, tym większe stają się trudności z przewidzeniem jej dalszego ruchu.
Formalne wyjaśnienie — fala, pakiet falowy i komutator
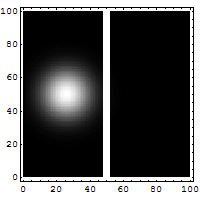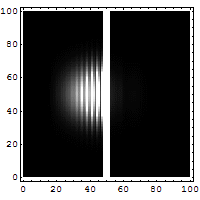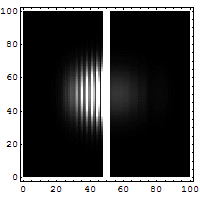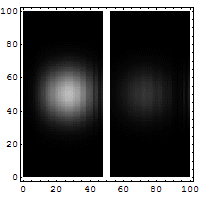
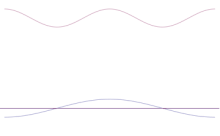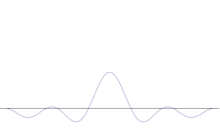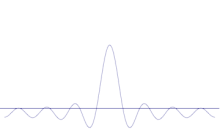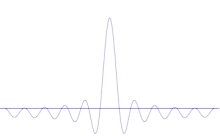
W mechanice kwantowej cząstkę opisuje funkcja falowa. Pozycja odpowiada rozkładowi tej funkcji w przestrzeni, a pęd sposobowi, w jaki funkcja ta rozkłada się w przestrzeni odwrotnej (w tak zwanej przestrzeni pędów) — formalnie przez transformatę Fouriera. Jeśli funkcja falowa jest mocno skupiona w położeniu (mały Δx), to jej transformata jest rozciągnięta (duże Δp). To matematyczne powiązanie tłumaczy nierówność Δx·Δp ≥ ħ/2.
Również z formalnego punktu widzenia nieoznaczoność wynika z faktu, że operatory pozycji i pędu nie przemieniają się (są niekomutujące). Ich komutator ma wartość [x, p] = iħ, co prowadzi do ograniczeń na jednoczesne przygotowanie stanów o dowolnie małych niepewnościach tych wielkości.
Praktyczne konsekwencje i zastosowania
Nieoczekiwane konsekwencje niepewnej cechy natury mają realne zastosowania i wyjaśniają wiele obserwowanych zjawisk:
- Rozszczepienie jądra atomowego — zrozumienie dynamiki i stabilności jąder atomowych wykorzystuje zasady mechaniki kwantowej, w tym ograniczenia wynikające z niepewności.
- Tunelowanie kwantowe — efekt, w którym cząstki „przechodzą” przez bariery energetyczne, jest bezpośrednio związany ze strukturą falową cząstek i nieoznaczonością; zjawisko to jest kluczowe dla działania diod tunelowych, tranzystorów i wielu elementów półprzewodnikowych w nowoczesnej elektronice.
Dlaczego nie widzimy efektu w skali codziennej?
Różnica między światem makro a mikro wynika z wartości stałej Plancka — ħ jest ekstremalnie małe (≈1,05·10^-34 J·s). Przykład liczbowy dobrze to ilustruje:
- Dla samochodu o masie ~1000 kg, jeśli założymy, że jego pozycję znamy z dokładnością Δx = 1 μm (10^-6 m), minimalna niepewność pędu wynosi Δp ≥ ħ/(2Δx) ≈ 5·10^-29 kg·m/s. To odpowiada niepewności prędkości Δv ≈ 5·10^-32 m/s — zupełnie nieistotnej w praktyce.
- Dla elektronu (masa ≈9,11·10^-31 kg) z lokalizacją na długości rzędu 1 Å (10^-10 m), to samo równanie daje Δp ≈ 5·10^-25 kg·m/s, co przekłada się na Δv rzędu 10^5–10^6 m/s — czyli ogromną niepewność prędkości. Stąd efekty są istotne w skali atomowej.
Najważniejsze wnioski
Zasada niepewności Heisenberga nie mówi, że pomiary są po prostu niedoskonałe; mówi, że natura sama w sobie nie pozwala na jednoczesne, dowolnie dokładne określenie pewnych par wielkości (jak pozycja i pęd). Ma to konsekwencje zarówno teoretyczne, jak i praktyczne — od podstawowych eksperymentów kwantowych (np. interferencja, pomiary „której drogi”) po technologie oparte na zjawiskach kwantowych.
W praktyce, dla obiektów makroskopowych efekt ten jest zwykle pomijalny, ale dla atomów, elektronów i układów nanometrowych pozostaje centralnym aspektem opisu ich zachowania.