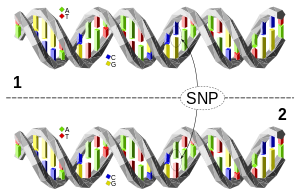
Pojedynczy polimorfizm nukleotydowy (SNP, wymawiany jako snip; liczba mnoga: snipy) to pojedyncza zmiana w sekwencji DNA występująca w populacji. SNP polega na wymianie jednego nukleotydu (A, T, C lub G) w genomie — na przykład krótkie fragmenty DNA dwóch osób AAGCCTA i AAGCTTA różnią się jednym nukleotydem. W takim przypadku mówimy o dwóch allelach tego miejsca. Większość powszechnych SNP ma tylko dwa allele.
Gdzie występują SNP i co o nich decyduje
SNP pojawiają się w całym genomie, zarówno w regionach kodujących (egzony), jak i niekodujących (introny, sekwencje regulatorowe, DNA pozagenowy). Najwięcej SNP znajduje się zwykle w obszarach, które nie powodują znaczących zaburzeń funkcji organizmu — gdyby zmiany te były silnie szkodliwe, zostałyby usunięte przez selekcję naturalną. Na gęstość i rozmieszczenie SNP wpływają także procesy takie jak rekombinacja genetyczna czy tempo powstawania nowych mutacji (mutacje).
Rodzaje i konsekwencje funkcjonalne
- SNP synonimiczne — zmiana nukleotydu w kodonie niezmieniająca aminokwasu; zazwyczaj bez wpływu na funkcję białka.
- SNP niesynonimiczne (missense) — zmiana prowadząca do innego aminokwasu, co może modyfikować funkcję białka.
- SNP nonsensowne — tworzące kodon stop, co zwykle skraca białko i może być szkodliwe.
- SNP w miejscach splice — mogą zaburzać składanie (splicing) mRNA i zmieniać produkt genowy.
- SNP w regionach regulatorowych (promotory, enhancery) — mogą wpływać na poziom ekspresji genów.
Częstość i różnice między populacjami
W populacjach mówi się o częstości allela mniejszościowego (MAF — minor allele frequency). SNP o MAF powyżej ~1% traktuje się zwykle jako wariant powszechny, natomiast poniżej tego progu — jako rzadki. Występowanie i częstość konkretnych alleli SNP różnią się między populacjami — allel powszechny w jednej grupie etnicznej może być rzadki w innej. Te różnice są wykorzystywane w badaniach populacyjnych i w analizach pochodzenia.
Metody wykrywania SNP
- Tablice SNP (SNP arrays) — szybkie i tanie testy dla setek tysięcy wybranych SNP; powszechnie stosowane w badaniach populacyjnych i klinicznych.
- Sekwencjonowanie następnej generacji (NGS) — wykrywa zarówno znane, jak i nowe SNP w całym genomie lub w wybranych regionach (exome, panel genów).
- Metody pojedynczych odczytów (np. Sanger) — użyteczne do walidacji wariantów.
Zastosowania praktyczne
- Kryminalistyka i identyfikacja — różnice genetyczne między osobami (szczególnie w niekodujących częściach genomu) są wykorzystywane przy fingerprintingu DNA w śledztwach kryminalnych.
- Badania asocjacyjne (GWAS) — porównywanie częstości SNP u chorych i zdrowych w celu identyfikacji loci związanych z cechami lub chorobami.
- Farmakogenomika — SNP mogą modulować odpowiedź na leki, co jest wykorzystane przy dobieraniu terapii.
- Diagnostyka i prognoza — niektóre SNP zwiększają ryzyko chorób lub wpływają na ich przebieg; przykładowo pojedyncza zmiana w genie APOE (apolipoproteina E) związana jest z wyższym ryzykiem choroby Alzheimera.
- Badania populacyjne i genealogia — analiza SNP służy do odwzorowywania historii migracji, pokrewieństwa i pochodzenia etnicznego.
Linkage disequilibrium i tag‑SNPy
SNPy często występują w grupach powiązanych (haplotypach) — zmiany w pobliskich miejscach mogą być skorelowane (linkage disequilibrium). To umożliwia stosowanie tzw. tag‑SNPów: wybranych markerów reprezentujących większe bloki wariantów, co zmniejsza liczbę koniecznych genotypowań w badaniach asocjacyjnych.
Bazy danych i zasoby
Istnieją publiczne bazy i katalogi SNP, które gromadzą informacje o zidentyfikowanych wariantach, ich częstościach i doniesieniach klinicznych (np. dbSNP, 1000 Genomes, gnomAD). Te zasoby pomagają interpretować wyniki badań genetycznych i oceniać, czy dany wariant jest powszechny czy rzadki.
Ograniczenia i kwestie etyczne
- SNP dają często tylko statystyczne skojarzenia z chorobami — nie zawsze wskazują na bezpośrednią przyczynę. Wiele efektów jest niewielkich, a predykcja ryzyka dla jednostki może być ograniczona.
- Interpretacja danych genetycznych wymaga ostrożności: populacyjne różnice, efekt środowiska i interakcje gen‑gen wpływają na wyniki.
- Kwestie prywatności i etyki — dane SNP mogą ujawniać informacje o pochodzeniu, zdrowiu i podatnościach; konieczne jest zabezpieczenie i świadoma zgoda na testy genetyczne.
Podsumowanie
SNP to najczęstsza forma zmienności genetycznej u ludzi i innych organizmów. Choć pojedyncza zmiana nukleotydu może mieć niewielkie konsekwencje, w skali genomu i populacji SNP są potężnym narzędziem do badania chorób, historii populacji, odpowiedzi na leki i identyfikacji. Rozwój technologii sekwencjonowania i zasobów baz danych znacząco zwiększył nasze możliwości wykrywania i interpretowania tych wariantów, przy jednoczesnym koniecznym uwzględnieniu ograniczeń i kwestii etycznych.