W chemii, siły van der Waalsa są rodzajem siły międzycząsteczkowej. Siła międzycząsteczkowa jest stosunkowo słabą siłą, która utrzymuje cząsteczki razem. Siły van der Waalsa są najsłabszym typem siły międzycząsteczkowej. Zostały one nazwane na cześć holenderskiego naukowca Johannesa Diderika van der Waalsa (1837–1923).
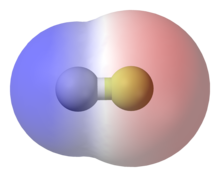
Mechanizm: w cząsteczkach elektrony nie są rozmieszczone zawsze w sposób idealnie symetryczny. W każdym momencie może powstać krótkotrwały, niejednolity rozkład ładunku — tzw. chwilowy dipol. Taki chwilowy dipol może indukować dipol w sąsiedniej cząsteczce, co prowadzi do przyciągania. Rozkłady ładunku mogą też być stałe (w cząsteczkach polarnych) i wtedy działają siły między stałymi dipolami. Te nieznaczne różnice w ładunku określamy jako ładunki częściowe, zapisywane jako δ- lub δ+.
Termin ten bywa czasem używany luźno jako synonim wszystkich sił międzycząsteczkowych, ale precyzyjnie obejmuje przede wszystkim słabsze interakcje pochodzące od dipoli i indukowanych dipoli. Siły van der Waalsa są słabsze od wiàzań kowalencyjnych i jonowych, lecz pełnią kluczową rolę w wielu zjawiskach: chemii supramolekularnej, enzymach, nauce o polimerach, nanotechnologii, nauce o powierzchni i fizyce materii skondensowanej. Określają także wiele właściwości związków organicznych, m.in. ich rozpuszczalność, temperatury topnienia i wrzenia oraz adhezję między ciałami.
- Główne typy sił van der Waalsa:
- siły Londona (dyspersyjne) — wynikają z chwilowych dipoli i są obecne we wszystkich cząsteczkach; dominują w gazach szlachetnych i niepolarnych związkach;
- siły Debye'a (dipol–indukowany dipol) — powstają, gdy dipol stały indukuje dipol w pobliskiej cząsteczce;
- siły Keesoma (dipol–dipol) — występują między cząsteczkami posiadającymi trwałe dipole i zależą od orientacji cząsteczek.
- Większe i silniejsze, ale nadal niekowalencyjne: dość często oddzielnie wyróżnia się także wiązanie wodorowe — silniejszą formę oddziaływania międzymolekularnego, o charakterze częściowo elektrostatycznym i częściowo kowalencyjnym; bywa traktowane jako specjalny przypadek sił van der Waalsa ze względu na jego międzycząsteczkowy charakter.
Zależność od odległości i wielkości cząsteczek: siły dyspersyjne zmniejszają się bardzo szybko wraz ze wzrostem odległości (w modelach matematycznych średnie przyciąganie opisuje się zależnością proporcjonalną do 1/r^6). W praktyce używa się często potencjału Lennarda–Jonesa (model 12–6), który opisuje krótkozasięgowe odpychanie i długozasięgowe przyciąganie między cząsteczkami.
Czynniki wpływające na siłę: polarizowalność (łatwość „przesunięcia” elektronów) rośnie z liczbą atomową i rozmiarem elektronowego obłoku, więc cięższe atomy i większe powierzchnie molekularne wykazują silniejsze oddziaływania dyspersyjne. Kształt i powierzchnia kontaktu także mają znaczenie — długie łańcuchy węglowodorowe wykazują większe oddziaływania między sobą niż rozgałęzione o tej samej masie molowej.
- Przykłady i znaczenie praktyczne:
- skraplanie gazów szlachetnych (np. argon, neon) jest możliwe dzięki siłom Londona;
- wzrastające temperatury wrzenia alkanów wraz z długością łańcucha wynikają głównie z większych sił dyspersyjnych;
- właściwości mechaniczne i adhezja w nanomateriałach i powłokach wynikają w dużej mierze z oddziaływań van der Waalsa (np. gecko wykorzystuje je do przylegania);
- składanie białek i interakcje enzym–substrat w dużym stopniu zależą od kombinacji sił van der Waalsa i oddziaływań elektrostatycznych;
- warstwy grafenu i materiały warstwowe są związane ze sobą siłami van der Waalsa, co umożliwia ich eksfoliację (rozdzielanie na pojedyncze warstwy).
Rozróżnienie od wiązań chemicznych: w odróżnieniu od wiązań kowalencyjnych czy jonowych, siły van der Waalsa nie tworzą nowych orbitalów ani całkowicie nie zmieniają elektronowej struktury atomów — są to zjawiska fizyczne między istniejącymi dipolami lub elektronowymi chmurami. Dlatego są zwykle odwracalne i zależne od temperatury i odległości.
W praktyce badawczej i inżynieryjnej rozumienie i kontrola sił van der Waalsa są istotne przy projektowaniu rozpuszczalników, surfaktantów, materiałów adhezyjnych, nanostruktur i układów supramolekularnych. Modele te są także podstawą symulacji molekularnych i opisu fazy skondensowanej materii.
Podsumowanie: choć są stosunkowo słabe w porównaniu z wiązaniami chemicznymi, siły van der Waalsa determinują wiele makroskopowych własności substancji (temperatury wrzenia, rozpuszczalność, adhezję, strukturę materiałów) i stanowią fundament zrozumienia zachowania układów od cząsteczkowego do materiałowego.

