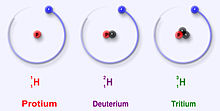
Wodór ma trzy główne izotopy: prot (1H), deuter (2H) i tryt (3H). Izotopy te powstają naturalnie w przyrodzie. Prot i deuter są stabilne. Tryt jest radioaktywny, a jego okres połowicznego rozpadu wynosi około 12 lat. Naukowcy stworzyli cztery inne izotopy wodoru (od 4H do 7H), ale są one bardzo niestabilne i nie występują naturalnie.
Budowa jądra i różnice masowe
- Prot (1H): jądro składa się z jednego protonu i nie zawiera neutronów; jest to najlżejszy i najpowszechniejszy izotop wodoru. - Deuter (2H)): jądro zawiera jeden proton i jeden neutron; masa jądrowa jest ~2 razy większa niż protu. - Tryt (3H): jądro zawiera jeden proton i dwa neutrony; jest cięższy od deuteru i niestabilny.
Różnice masowe wpływają na własności fizyczne i chemiczne związków wodoru (np. częstotliwości drgań wiązań, stałe szybkości reakcji, punkty topnienia i wrzenia), co wykorzystuje się m.in. w badaniach izotopowych i analizie kinetyki reakcji.
Występowanie i naturalna obfitość
Najczęściej spotykanym izotopem jest prot — stanowi zdecydowaną większość wodoru w przyrodzie. Deuter występuje naturalnie w bardzo małych ilościach (rzędu kilkuset części na milion atomów wodoru, ok. 0,015% masowo), tworząc m.in. ciężką wodę (D2O). Tryt w przyrodzie występuje w śladowych ilościach — powstaje m.in. w atmosferze wskutek interakcji promieniowania kosmicznego z azotem oraz w reaktorach jądrowych; z uwagi na krótszy okres półtrwania jego ilości są niewielkie.
Właściwości chemiczne i fizyczne
- Chemicznie wszystkie izotopy zachowują się bardzo podobnie (mają po jednym elektronie), ale efekty izotopowe wpływają na szybkości reakcji i siłę wiązań.
- Cięższe izotopy powodują zmiany energetyczne w wiązaniach: np. D–H/D–O są silniejsze i mają niższe częstotliwości drgań niż H–O.
- Właściwości makroskopowe związków różnią się nieznacznie — przykładowo ciężka woda D2O ma wyższy punkt wrzenia, gęstość i inną przewodność niż zwykła woda.
Zastosowania
- Deuter: stosowany jako znacznik izotopowy w badaniach chemicznych i biologicznych (tracing), jako rozpuszczalnik do spektroskopii NMR (D2O) oraz w syntezach izotopowo znakowanych związków.
- Ciężka woda (D2O): używana jako moderator neutronów w niektórych typach reaktorów jądrowych oraz w badaniach fizycznych i chemicznych.
- Tryt: stosowany w źródłach światła luminescencyjnego (np. znaki awaryjne), jako znacznik w badaniach biologicznych i chemicznych oraz jako paliwo do badań nad fuzją jądrową (reakcje D–T). Ze względu na radioaktywność tryt ma też zastosowania w technologiach jądrowych i w monitoringu środowiska.
Bezpieczeństwo i własności trytu
Tryt jest radioaktywny i ulega rozpadowi beta minus, przekształcając się w jądrze w helu-3. Jego okres półtrwania wynosi około 12 lat (okres połowicznego rozpadu). Promieniowanie beta emitowane przez tryt ma niską energię i nie penetruje skóry, głównym zagrożeniem jest jednak wciągnięcie go do organizmu (woda zawierająca tryt, inhalacja, spożycie). W praktyce stosuje się procedury ograniczające narażenie i monitorowanie stężeń trytu w środowisku oraz produktach przemysłowych.
Inne izotopy wodoru (4H–7H)
Naukowcy wytworzyli eksperymentalnie izotopy od 4H do 7H, ale są one ekstremalnie niestabilne — obserwowane jedynie w reakcjach jądrowych i rozpadają się bardzo szybko. Nie występują naturalnie w środowisku i nie mają praktycznych zastosowań ze względu na bardzo krótki czas życia.
Uwagi dotyczące nazewnictwa
Główne izotopy wodoru są wyjątkowe tym, że mają własne nazwy: prot, deuter i tryt. Nazwy te są powszechnie używane i dla deuteru oraz trytu często spotyka się również symbole alternatywne D i T. Międzynarodowa Unia Chemii Czystej i Stosowanej zaleca używanie notacji z liczebnikiem masowym (np. 2H, 3H) dla pełnej jednoznaczności, jednak symbole D i T pozostają szeroko stosowane w literaturze i praktyce.