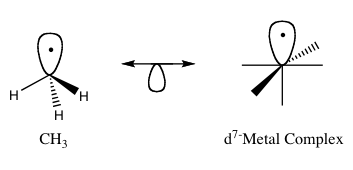
Zasada izolobalna (znana również jako analogia izolobalna) jest sposobem na przewidywanie właściwości wiążących związków metaloorganicznych. W chemii organometalicznej odnosi się ona do struktury ligandów organicznych, które mogą wiązać się z nieorganicznymi fragmentami molekularnymi. Roald Hoffmann opisał fragmenty molekularne jako izolobalne "jeśli liczba, właściwości symetryczne, przybliżona energia i kształt orbitali granicznych i liczba elektronów w nich jest podobna - nie identyczna, ale podobna". W praktyce oznacza to, że wiązanie i reaktywność mniej znanych fragmentów można przewidzieć od fragmentów lepiej poznanych, jeśli dwa fragmenty molekularne mają podobne orbity graniczne, najwyżej zajmowaną orbitę molekularną (HOMO) i najniżej zajmowaną orbitę molekularną (LUMO). Związki izolobalowe są analogami do związków izoelektronicznych, które mają taką samą liczbę elektronów walencyjnych i podobną strukturę przestrzenną, jednak izolobalność odnosi się bardziej do podobieństwa orbitali brzegowych niż do dokładnej równości liczby elektronów czy identycznej struktury. Graficzne przedstawienie struktur izolobalnych, z parami izolobalnymi połączonymi za pomocą dwugłowicowej strzałki z połową orbity poniżej, znajduje się na rysunku 1.
Na czym polega użyteczność zasady?
Zasada izolobalna dostarcza prostego, intuicyjnego modelu do:
- przewidywania, jak fragmenty organiczne i metaloorganiczne mogą się łączyć,
- rozumienia struktury i geometrii kompleksów,
- projektowania nowych ligandów i klastrów metaloorganicznych oraz proponowania mechanizmów reakcji katalitycznych.
Typowe zastosowania i przykłady
W literaturze i praktyce organometalurgicznej zasada bywa używana do:
- porównywania grup alkilowych lub arylowych z odpowiednimi fragmentami metalicznymi,
- uzasadniania powstawania określonych układów mostkowych i klastrowych,
- projektowania kompleksów o zadanej liczbie wiązań i przewidywania ich elektronowej struktury,
- wspomagania interpretacji wyników obliczeń kwantowo‑chemicznych (np. DFT) i spektroskopii poprzez korelowanie kształtów orbit.
Ograniczenia i uwagi praktyczne
Mimo użyteczności, analogia izolobalna ma swoje ograniczenia:
- Jest modelem jakościowym — nie zawsze daje precyzyjne prognozy ilościowe dotyczące energii czy szybkości reakcji.
- Podobieństwo orbitali musi uwzględniać energię i symetrię; drobne różnice energetyczne lub wpływ ligandów otaczających mogą zmienić zachowanie fragmentów.
- Nie uwzględnia efektów sterycznych, solwatacji ani dynamicznych zmian w układzie, które w praktyce mogą zdominować chemiczne właściwości.
- W niektórych przypadkach analogia zawodzi — szczególnie gdy elektroniczne lub steryczne czynniki drugorzędne są znaczące.
Historia i znaczenie
Za pracę nad izolacyjną analogią Roald Hoffmann otrzymał w 1981 roku Nagrodę Nobla w dziedzinie chemii, którą dzielił z Kenichi Fukui. W swoim wykładzie o Nagrodzie Nobla Hoffmann podkreślił, że izolobalna analogia jest użytecznym, a zarazem prostym modelem. W niektórych przypadkach zawodzi, ale pozostaje ważnym elementem myślenia chemików zajmujących się związkami metaloorganicznymi i mechanizmami reakcji, ponieważ łączy pojęcia orbitali molekularnych z intuicją chemiczną.
Uwaga praktyczna: aby w pełni wykorzystać analogię izolobalną, chemicy często łączą ją z obliczeniami kwantowo‑chemicznymi (np. DFT), analizą spektroskopową i eksperymentami strukturalnymi — wtedy model służy jako punkt wyjścia do dokładniejszych badań.