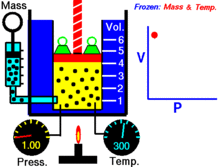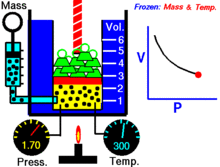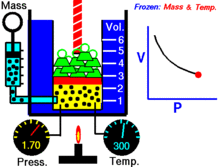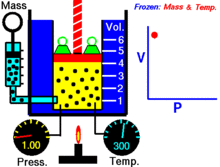
Prawo Boyle'a (zwane również prawem Mariotte'a i prawem Boyle'a–Mariotte'a) opisuje zachowanie idealnych gazów przy stałej temperaturze i stałej ilości gazu.
Dla stałej ilości gazu idealnego utrzymywanej w stałej temperaturze, P (ciśnienie) i V (objętość) są odwrotnie proporcjonalne.
Wzór i interpretacja
Innymi słowy: przy stałej masie gazu i stałej temperaturze iloczyn ciśnienia i objętości jest stały. Matematycznie zapisujemy to jako proporcję:
P ∝ 1 V {\i1}propto {\i1}frac {\i1}{\i1}
albo równoważnie:
P V = k {\i1}- styropian PV=k
gdzie P jest ciśnieniem gazu, V jest objętością gazu, a k jest stałą (dla danej masy gazu w danej temperaturze).
Postać użyteczna do obliczeń
Porównując dwa stany tego samego gazu (te same n i T) otrzymujemy:
P 1 V 1 = k {\i1}styk stylistyczny P_{1}V_{1}=k}
P 2 V 2 = k {\i1}styk stylistyczny P_{2}V_{2}=k}
Ponieważ k jest takie samo w obu stanach, otrzymujemy znany związek:
P 1 V 1 = P 2 V 2 {\i1}V_{1}=P_{2}V_{2}}}
Przykład obliczeniowy
Przykład: Ciśnienie początkowe P1 = 3 atm, objętość początkowa V1 = 5 l. Jeśli ciśnienie zmniejsza się do P2 = 2 atm, jaka będzie objętość V2?
P 1 V 1 = P 2 V 2 {\i1}V_{1}=P_{2}V_{2}}}
Stąd:
V 2 = P 1 V 1 P 2 {\i1}== {\i1}frac {\i1}V_{\i1}}{P_{\i1}V_{\i0}
V 2 = 3 ∗ 5 2 {\i1}== {\i1}frac {3*5}{2}}
V 2 = 15 2 {\i1}{\i1}Styl V_{\i0}== {\i1}frac {\i1}{\i1}
V 2 = 7.5 {\i1} {\i1}Style V_{\i0}=7.5}
∴ Obj ętość wyniesie 7,5 litra (przy założeniu, że temperatura pozostaje niezmieniona).
Wyprowadzenie z równania stanu gazu doskonałego
Prawo Boyle'a można łatwo otrzymać z równania stanu gazu idealnego:
PV = nRT
Dla stałej ilości moli n oraz stałej temperatury T prawy człon równania nRT jest stały, więc PV = const, co jest właśnie treścią prawa Boyle'a.
Interpretacja mikroskopowa (kinetyczna)
W ujęciu kinetycznym zmniejszając objętość przy tej samej liczbie cząstek i tej samej średniej energii kinetycznej (stała temperatura), cząsteczki częściej zderzają się ze ściankami naczynia — rośnie liczba zderzeń na jednostkę powierzchni i w rezultacie rośnie ciśnienie. Stąd odwrotna proporcjonalność P ∝ 1/V.
Graficzne przedstawienie
Dla stałej temperatury wykres zależności V od P (lub P od V) jest gałęzią hiperboli na wykresie PV = const. Iloczyn P·V pozostaje taki sam dla każdej pary punktów na tej hiperboli.
Zastosowania praktyczne
- strzykawki i pompy tłokowe (zmiana objętości prowadzi do zmiany ciśnienia),
- silniki tłokowe — część cyklu przemian gazów w cylindrze,
- badania gazów w laboratoriach (określanie objętości przy znanym ciśnieniu),
- zjawiska meteorologiczne i inżynieria (w praktyce uwzględnia się również inne czynniki, np. zmiany temperatury).
Ograniczenia i uwagi praktyczne
- Prawo Boyle'a jest prawdziwe dla gazów idealnych — w rzeczywistości przy bardzo wysokich ciśnieniach lub niskich temperaturach (gdzie oddziaływania międzycząsteczkowe stają się istotne) gazy odbiegają od tego prawa.
- Należy pamiętać o jednostkach: P i V muszą być wyrażone w spójnych jednostkach (np. atm i l przy obliczeniach względnych albo Pa i m3 w układzie SI). Jeśli używamy ciśnień względnych (manometrycznych), trzeba uważać — zwykle w takich obliczeniach używa się ciśnienia absolutnego.
- Prawo obowiązuje tylko wtedy, gdy temperatura pozostaje stała (proces izotermiczny). Jeśli podczas zmiany objętości następuje ogrzewanie lub ochładzanie gazu, stosujemy pełne równanie stanu lub analizę termodynamiczną odpowiedniego procesu.
Krótka wzmianka historyczna
Prawo odkrył Robert Boyle w 1662 roku; niezależnie zaobserwował je także Edme Mariotte (ok. 1679). Stąd nazwa prawa Boyle'a–Mariotte'a.