Krystalografia rentgenowska to metoda umożliwiająca poznanie trójwymiarowego rozmieszczenia atomów w cząsteczkach i ciałach stałych. Dzięki niej można „zobaczyć” strukturę na poziomie atomowym — od małych związków organicznych i nieorganicznych po duże makromolekuły biologiczne, takie jak białka czy kwasy nukleinowe. W praktyce promieniowanie rentgenowskie oddziałuje z chmurą elektronów atomów próbki i zostaje przez nią rozproszone; to rozproszenie tworzy charakterystyczny wzór (dyfrakcję), z którego po przetworzeniu można odtworzyć „obraz” rozkładu elektronów i w efekcie położenie atomów.
Zasada działania — jak powstaje obraz
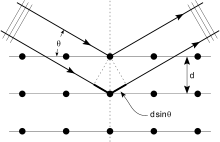
W krystalografii rentgenowskiej badana próbka powinna tworzyć uporządkowaną strukturę krystaliczną, bo regularne ułożenie atomów powoduje ukierunkowane wzmacnianie i wygaszanie fal rozproszonych (interferencję). Najprostszym opisem zjawiska jest prawo Bragga, które w słowach mówi: promieniowanie padające na płaszczyzny atomowe kryształu ulega wzmocnieniu w określonych kątach. W zapisie matematycznym: n·λ = 2 d · sin θ (gdzie n to rząd dyfrakcji, λ długość fali promieniowania, d odległość między płaszczyznami sieci, a θ kąt padania/odbicia). Intensywność i pozycje prążków (punktów) dyfrakcyjnych rejestruje detektor — z tych danych za pomocą obliczeń uzyskuje się mapy elektronowe, na podstawie których buduje się model atomowy.
Główne warianty techniki
- Dyfrakcja rentgenowska na pojedynczym krysztale (Single-crystal XRD) — daje dokładne, trójwymiarowe struktury molekularne; wymaga uzyskania pojedynczych kryształów odpowiedniej jakości.
- Dyfrakcja proszkowa (Powder XRD) — stosowana, gdy materia występuje w postaci drobnego proszku; użyteczna do identyfikacji faz, określania parametrów sieci i analizy ilościowej mieszanin (np. metoda Rietvelda).
- Krystalografia makromolekularna — specjalizacja dla białek, kwasów nukleinowych i kompleksów biologicznych; często wykorzystuje techniki kriogeniczne i synchrotronowe źródła promieniowania.
Typowy przebieg badania
Proces badania struktury obejmuje kilka etapów:
- uzyskanie próbki i (jeśli to konieczne) wyhodowanie kryształów,
- montaż kryształu na goniometrze i naświetlanie promieniami rentgenowskimi,
- rejestracja danych dyfrakcyjnych przez detektor,
- obróbka i przetwarzanie danych (indeksacja, integracja intensywności),
- rozwiązanie problemu faz (np. metoda jedno- lub wielocząsteczkowa — SAD, MAD, MIR — lub metoda podstawienia molekularnego),
- budowa modelu atomowego, jego dopasowanie (refinment) i walidacja jakości struktury.
Metody rozwiązania tzw. problemu faz
Detektory rejestrują jedynie intensywności rozproszonego światła, a nie jego fazy — dlatego konieczne są dodatkowe metody odtworzenia informacji fazowej. Najczęściej stosowane podejścia to:
- Metody empiryczne (np. izomorficzne podstawienie — MIR),
- Metody wykorzystujące zależności energetyczne (MAD, SAD - anomaliczne rozproszenie),
- Podstawienie molekularne (molecular replacement) — gdy znana jest struktura blisko spokrewnionego związku.
Historia i znaczące odkrycia
Technikę zaproponowali wspólnie Sir William Bragg (1862–1942) i jego syn Sir Lawrence Bragg (1890–1971). Za rok 1915 otrzymali Nagrodę Nobla z fizyki za badania nad strukturą kryształów dzięki zastosowaniu promieni rentgenowskich — Lawrence Bragg jest najmłodszym laureatem Nagrody Nobla. To właśnie w kontekście rozwoju technik krystalograficznych Laboratorium Cavendisha na Uniwersytecie Cambridge, którym kierował Lawrence Bragg, stało się miejscem kluczowych prac nad strukturą DNA — odkrycie struktury dwuniciowej przypisuje się zespołowi James D. Watson, Francis Crick, Maurice Wilkins i Rosalind Franklin (luty 1953).
Nowoczesne rozwinięcia techniki
Od czasów Braggów technika znacznie się rozwinęła. Do najważniejszych postępów należą:
- zastosowanie potężnych, synchrotronowych źródeł promieniowania — pozwalają na krótszy czas pomiaru i lepszą jakość danych,
- detektory szybkie i o wysokiej czułości (np. detektory pikselowe),
- kriokrystalografia — zamrażanie kryształów do niskich temperatur w celu ograniczenia uszkodzeń radiacyjnych,
- użycie laserowych i wolnoelektronowych źródeł (XFEL) do badania dynamiki struktur i badania bardzo małych kryształów.
Zastosowania
Krystalografia rentgenowska ma szerokie zastosowania w nauce i przemyśle:
- w chemii — określanie struktury nowych związków i potwierdzanie stereochemii,
- w biologii i biochemii — poznawanie struktur białek, enzymów i kompleksów biologicznych, co jest kluczowe w projektowaniu leków,
- w farmacji — charakterystyka form krystalicznych substancji czynnych, kontrola czystości i badanie polimorfizmu,
- w materiałoznawstwie — analiza struktury materiałów, katalizatorów, półprzewodników czy materiałów energetycznych (baterie, ogniwa),
- w geologii i mineralogii — identyfikacja minerałów i ich parametrów sieci,
- w konserwacji dzieł sztuki i kryminalistyce — analiza składników i metod wytwarzania.
Ograniczenia i problemy praktyczne
Choć krystalografia jest niezwykle potężnym narzędziem, ma też ograniczenia:
- konieczność uzyskania kryształów o wystarczającej jakości (dla niektórych związków jest to trudne lub niemożliwe),
- uszkodzenia radiacyjne — silne promieniowanie może powodować degradację delikatnych próbek; w krystalografii makromolekularnej stosuje się wtedy chłodzenie kriogeniczne,
- problem fazowy — wymaga dodatkowych procedur lub znanych wzorców do jego rozwiązania,
- analiza struktur o dużej nieuporządkowanej części (np. fragmenty białek bez stałej konformacji) bywa utrudniona.
Oprogramowanie i analiza danych
Po zarejestrowaniu danych konieczne jest ich przetworzenie i dopracowanie modelu strukturalnego. Typowe programy i pakiety używane w krystalografii to m.in. SHELX, CCP4, PHENIX, Coot oraz komercyjne narzędzia do refinamentu i walidacji. Wynik końcowy poddaje się rygorystycznej walidacji jakości (np. parametry R, geometria, gęstości elektronowej), aby ocenić wiarygodność modelu.
Podsumowując: krystalografia rentgenowska to jedno z najważniejszych narzędzi współczesnej nauki, pozwalające zobaczyć materię na poziomie atomowym. Dzięki ciągłym postępom w źródłach promieniowania, detekcji i oprogramowaniu jej znaczenie w chemii, biologii, naukach materiałowych i przemyśle wciąż rośnie.