Synapsy chemiczne to synapsy, które do przekazywania sygnałów używają chemicznych posłańców zwanych neuroprzekaźnikami. Znajdują się one w całym organizmie, a szczególnie liczne i złożone są w centralnym układzie nerwowym i w mózgu. Synapsy chemiczne pośredniczą w komunikacji między komórkami nerwowymi (neuronami) i między neuronami a komórkami efektorowymi (np. mięśniowymi czy gruczołowymi).
Neurony wykorzystują sygnały elektryczne do przenoszenia informacji — są to potencjały czynnościowe. Szacuje się, że w przeciętnym ludzkim mózgu znajduje się około 86 miliardów neuronów. Neurony nie działają samodzielnie: muszą się łączyć i wymieniać informacje. Ponieważ sygnał elektryczny nie może bezpośrednio „przeskoczyć” szczeliny synaptycznej w synapsie chemicznej, konieczne są neuroprzekaźniki, które przenoszą informację z jednego neuronu do drugiego. W przeciwieństwie do synaps elektrycznych, gdzie przekaz jest bezpośrednio elektryczny, synapsy chemiczne wykorzystują mechanizmy wydzielnicze i receptorowe. Synapsy chemiczne można klasyfikować według funkcji (np. pobudzające vs hamujące) i struktury (np. osadzone na dendrytach, ciele komórkowym lub na kolcach dendrytycznych).
Budowa synapsy chemicznej
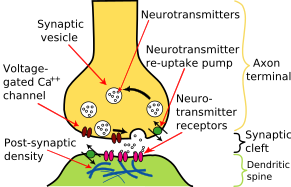
Typowa synapsa chemiczna składa się z trzech elementów: presynaptycznego zakończenia (bouton) zawierającego pęcherzyki synaptyczne z neuroprzekaźnikiem, szczeliny synaptycznej (przestrzeni międzykomórkowej, zwykle ~20–40 nm) oraz postsynaptycznego zagęszczenia na błonie komórkowej neuronu odbiorczego, zawierającego receptory. W zakończeniu presynaptycznym znajdują się także białka odpowiedzialne za transport i fuzję pęcherzyków (np. białka SNARE, synaptotagmina) oraz kanały wapniowe zależne od napięcia.
Mechanizm działania — krok po kroku
- Napływ impulsu: Potencjał czynnościowy dociera do zakończenia presynaptycznego i depolaryzuje błonę.
- Otwieranie kanałów Ca2+: Depolaryzacja otwiera napięciowo zależne kanały wapniowe, a jon Ca2+ napływa do wnętrza zakończenia.
- Fuzja pęcherzyków: Wzrost stężenia Ca2+ inicjuje połączenie pęcherzyków synaptycznych z błoną presynaptyczną i egzocytozę neuroprzekaźnika do szczeliny synaptycznej.
- Dyfuzja i wiązanie: Neuroprzekaźnik dyfunduje przez szczelinę i wiąże się z receptorami na błonie postsynaptycznej.
- Odpowiedź postsynaptyczna: Zależnie od typu receptora (jonotropowy lub metabotropowy) następuje szybkie otwarcie kanałów jonowych (zmiana potencjału postsynaptycznego — EPSP lub IPSP) lub aktywacja kaskad metabolicznych i modulacja aktywności komórki.
- Zakończenie sygnału: Neuroprzekaźnik jest usuwany przez przechwytywanie zwrotne (reuptake), enzymatyczne rozkładanie (np. acetylocholinesteraza dla acetylocholiny), lub dyfuzję poza szczelinę, co kończy transmisję.
- Recykling pęcherzyków: Błona pęcherzyków jest odzyskiwana i wykorzystywana ponownie w cyklu synaptycznym.
Rodzaje receptorów i ich efekt
- Receptory jonotropowe — działają szybko, są kanałami jonowymi: np. NMDA, AMPA (dla glutaminianu) czy receptory nikotynowe (dla acetylocholiny).
- Receptory metabotropowe — sprzężone z białkami G, działają wolniej i modulują wewnątrzkomórkowe szlaki sygnałowe, wpływając na potencjał błonowy i ekspresję genów.
Neuroprzekaźniki — przykłady i funkcje
Neuroprzekaźniki można podzielić według budowy i funkcji. Do najważniejszych należą:
- Glutaminian — główny przekaźnik pobudzający w mózgu (ważny dla uczenia się i pamięci).
- GABA — główny przekaźnik hamujący, kluczowy dla kontroli pobudliwości neuronalnej.
- Acetylocholina — zaangażowana w przekazywanie w synapsach nerwowo‑mięśniowych i w funkcje kognitywne.
- Dopamina, serotonina, noradrenalina — neuromodulatory wpływające na nastrój, motywację, uwagę i regulację procesów wewnątrz ośrodkowego układu nerwowego.
- Glicyna — hamujący neuroprzekaźnik w rdzeniu kręgowym.
Rodzaje synaps chemicznych
- Pobudzające — generują potencjały postsynaptyczne depolaryzujące (EPSP), zwiększając prawdopodobieństwo wywołania potencjału czynnościowego (np. synapsy glutaminergiczne).
- Hamujące — powodują hiperpolaryzację (IPSP), zmniejszając pobudliwość (np. synapsy GABA‑ergiczne).
- Modulujące — neuromodulatory zmieniają ogólną wrażliwość i plastyczność sieci neuronowych (np. dopaminergiczne, serotoninergiczne).
Plastyczność synaptyczna i znaczenie
Synapsy chemiczne są elastyczne — ich siła może się zmieniać w odpowiedzi na aktywność, co jest podstawą uczenia się i pamięci. Dwa dobrze poznane zjawiska to:
- Wzmacnianie długotrwałe (LTP) — trwały wzrost efektywności synaptycznej najczęściej związany z aktywacją receptorów NMDA i napływem Ca2+, co prowadzi do zwiększenia liczby receptorów AMPA w błonie postsynaptycznej.
- Osłabienie długotrwałe (LTD) — długotrwałe zmniejszenie efektywności synaptycznej, również powiązane z wewnątrzkomórkowymi zmianami w zależności od wzorców aktywności.
Mechanizmy zakończenia sygnału i regulacja
Sposoby zakończenia działania neuroprzekaźników obejmują:
- Reuptake — wychwyt zwrotny przez transportery w błonie presynaptycznej lub komórkach glejowych (np. transportery serotoniny, dopaminy).
- Enzymatyczne rozkładanie — np. acetylocholinesteraza rozkłada acetylocholinę w szczelinie synaptycznej.
- Dyfuzja poza obszar synaptyczny.
Znaczenie kliniczne
Zaburzenia funkcji synaps chemicznych wiążą się z wieloma schorzeniami neurologicznymi i psychiatrycznymi: choroba Alzheimera (zaburzenia acetylocholiny), choroba Parkinsona (niedobór dopaminy), depresja (zaburzenia serotoniny/noradrenaliny) czy schizofrenia (zaburzenia przekaźnictwa dopaminergicznego/glutamatergicznego). Wiele leków terapeutycznych działa poprzez modulowanie synaptycznego przekazu:
- SSRI (selektywne inhibitory wychwytu serotoniny) zwiększają stężenie serotoniny w szczelinie synaptycznej.
- Benzodiazepiny wzmacniają działanie GABA (zwiększają przewodnictwo kanałów GABA_A).
- Toksyny, np. toksyna botulinowa, hamują uwalnianie neuroprzekaźników, prowadząc do porażenia mięśni.
Podsumowując, synapsy chemiczne to złożone mikrostruktur, które przekształcają sygnały elektryczne w chemiczne i z powrotem na elektryczne w komórce odbierającej. Dzięki mechanizmom receptoryjnym, regulacji i plastyczności umożliwiają one precyzyjną kontrolę funkcji układu nerwowego, uczenie się, pamięć oraz adaptację do zmieniających się warunków środowiskowych.