Autofagia (co oznacza "zjadanie siebie") jest jednym z podstawowych mechanizmów komórkowych. Pozwala ona na kontrolowany rozpad części komórki, które nie działają lub nie są potrzebne. Te części komórki mogą być następnie ponownie wykorzystane w razie potrzeby.
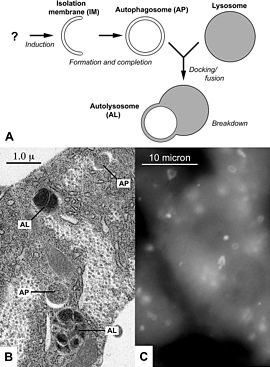
Dzieje się to na kilka sposobów. Ukierunkowane części komórki mogą być odizolowane od reszty komórki w autofagosomie (podwójnie zmembranizowanej cząsteczce). Autofagosom łączy się z lizosomem, a jego zawartość jest rozkładana i utylizowana. W skrajnym przypadku głodu, rozpad składników komórkowych sprzyja przetrwaniu komórki poprzez utrzymanie poziomu energii komórkowej.
Nazwa "autofagia" została ukuta przez belgijskiego biochemika Christiana de Duve w 1963 roku. Identyfikacja genów związanych z autofagią w drożdżach w latach 90. pozwoliła badaczom poznać mechanizmy autofagii. Doprowadziło to do przyznania w 2016 roku Nagrody Nobla w dziedzinie fizjologii lub medycyny japońskiemu badaczowi Yoshinori Ohsumi.
Mechanizm — krok po kroku
Podstawowy cykl autofagii (zwany też makroautofagią) można opisać w kilku etapach:
- Indukcja — sygnały stresowe (np. brak składników odżywczych, niedotlenienie, uszkodzenia organelli) uruchamiają szlaki aktywujące autofagię.
- Inicjacja i nucleacja — powstaje początkowa struktura błonowa (faza pre-autofagosomu), na którą składa się skoncentrowany kompleks białek regulujących tworzenie autofagosomu.
- Rozszerzanie i zamknięcie — błona otacza wyselekcjonowany materiał (np. uszkodzone mitochondria), tworząc zamknięty autofagosom.
- Fuzja z lizosomem — autofagosom łączy się z lizosomem, gdzie enzymy hydrolityczne rozkładają zawartość na proste związki.
- Recykling — powstałe aminokwasy, kwasy tłuszczowe i inne metabolity są uwalniane i wykorzystane ponownie przez komórkę.
Rodzaje autofagii
Autofagia nie jest jednorodnym procesem; wyróżnia się kilka typów:
- Makroautofagia — najbardziej opisany typ, obejmuje tworzenie autofagosomów i ich fuzję z lizosomami.
- Microautofagia — bezpośrednie wciąganie cytoplazmy przez błonę lizosomalną lub wakuolę.
- Autofagia zależna od chaperonów (CMA) — selektywne rozpoznawanie białek przez białka opiekuńcze (chaperony) i ich transport bezpośrednio przez błonę lizosomalną.
- Selektywna autofagia — np. mitofagia (usuwanie uszkodzonych mitochondriów), aggrefagia (usuwanie agregatów białkowych), xenofagia (eliminacja patogenów) — komórka rozpoznaje i usuwa konkretne przeszkody dla homeostazy.
Regulacja procesu
Autofagia jest skrupulatnie regulowana przez wiele szlaków sygnałowych. Najważniejsze to:
- mTOR — kluczowy inhibitor autofagii; w obecności obfitości składników odżywczych mTOR hamuje inicjację autofagii.
- AMPK — aktywowany przy niskim poziomie energii (wysoki stosunek AMP/ATP), promuje autofagię poprzez hamowanie mTOR i bezpośrednią aktywację elementów inicjujących autofagocytozę.
- Białka z rodziny ATG (autophagy-related genes) — warunkują skład i przebieg maszynerii tworzącej autofagosomy.
Znaczenie dla zdrowia i chorób
Autofagia pełni rolę ochronną, ale jej zaburzenia mają konsekwencje w wielu stanach chorobowych:
- Neurodegeneracja — niewydolność autofagii sprzyja akumulacji toksycznych agregatów białkowych (np. w chorobie Parkinsona, Alzheimera); poprawa autofagii może ułatwiać usuwanie takich agregatów.
- Nowotwory — rola autofagii w raku jest złożona: z jednej strony może chronić przed nowotworzeniem przez usuwanie uszkodzonych organelli i DNA, z drugiej strony komórki nowotworowe mogą wykorzystywać autofagię do przetrwania w warunkach stresu (np. niedotlenienia, terapii).
- Infekcje — autofagia (xenofagia) pomaga eliminować patogeny wewnątrzkomórkowe; niektóre mikroorganizmy potrafią jednak unikać lub wykorzystywać mechanizm dla własnych celów.
- Starzenie — z wiekiem aktywność autofagii zwykle maleje, co przyczynia się do kumulacji uszkodzonych komponentów komórkowych i pogorszenia funkcji tkanek; interwencje które poprawiają autofagię często przedłużają zdrowy okres życia w modelach zwierzęcych.
- Choroby metaboliczne — autofagia wpływa na metabolizm lipidów i glukozy; jej zaburzenia są powiązane z otyłością, insulinoopornością i stłuszczeniem wątroby.
Co pobudza i co hamuje autofagię?
- Pobudza: głodówka, ograniczenie kalorii, ćwiczenia fizyczne, aktywacja AMPK, niektóre leki (np. rapamycyna hamująca mTOR), stres oksydacyjny.
- Hamuje: obfitość składników odżywczych, silna aktywacja mTOR, niektóre czynniki prozapalne lub metaboliczne.
Badania i możliwości terapeutyczne
Naukowcy badają modulację autofagii jako strategię terapeutyczną. Przykłady obszarów badań:
- leki indukujące autofagię w chorobach neurodegeneracyjnych,
- hamowanie autofagii w wybranych nowotworach, aby zwiększyć wrażliwość komórek nowotworowych na chemioterapię,
- poprawa autofagii metabolicznej w chorobach wątroby i cukrzycy,
- wykorzystanie autofagii w walce z infekcjami wewnątrzkomórkowymi.
Jak w praktyce wspierać zdrową autofagię?
Chociaż mechanizmy są złożone, istnieją ogólne zalecenia sprzyjające prawidłowej aktywności autofagii:
- zdrowa dieta i okresowe ograniczenie kalorii/intermittent fasting (po konsultacji z lekarzem),
- regularna aktywność fizyczna,
- unikanie przewlekłego stresu i toksyn (np. nadmiernego spożycia alkoholu),
- badania nad lekami modulującymi autofagię trwają; stosowanie farmakoterapii powinno być oparte na dowodach i nadzorze medycznym.
Podsumowanie
Autofagia to uniwersalny, dynamiczny mechanizm komórkowy służący utrzymaniu homeostazy poprzez usuwanie i recykling niepotrzebnych lub uszkodzonych elementów. Ma kluczowe znaczenie dla przystosowania się komórki do stresu, ochrony przed chorobami i regulacji metabolizmu. Zrozumienie jej mechanizmów otwiera możliwości terapeutyczne w wielu chorobach, ale wymaga dalszych badań, by bezpiecznie i skutecznie modulować ten proces u ludzi.