Mikroskop fluorescencyjny to mikroskop optyczny, który wykorzystuje fluorescencję i fosforescencję do badania substancji organicznych lub nieorganicznych. "Mikroskop fluorescencyjny" oznacza każdy mikroskop, który wykorzystuje fluorescencję do tworzenia obrazu. Dotyczy to zarówno prostszych, jak i bardziej skomplikowanych konstrukcji.
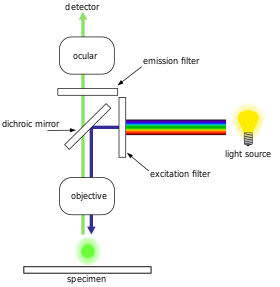
Większość mikroskopów fluorescencyjnych, szczególnie tych używanych w naukach przyrodniczych, ma budowę epifluorescencyjną przedstawioną na rysunku. Światło o długości fali wzbudzającej oświetla próbkę przez obiektyw. Fluorescencja emitowana przez próbkę jest ogniskowana na detektorze. Dichroiczny beamsplitter działa jak filtr o określonej długości fali, przepuszczając światło fluorescencyjne do okularu lub detektora, ale odbijając pozostałe światło wzbudzające z powrotem w kierunku źródła.
Co to jest fluorescencja i fosforescencja?
Fluorescencja to zjawisko emisji światła przez substancję bezpośrednio po absorpcji promieniowania o krótszej długości fali — emisja ustaje niemal natychmiast po odcięciu wzbudzenia. Fosforescencja natomiast cechuje się dłuższym opóźnieniem emisji (tzw. efektem długotrwałym) wynikającym z przejść zabronionych kwantowo-mechanicznie. W praktyce mikroskopii fluorescencyjnej częściej pracuje się z fluoroforami wykazującymi szybkie, intensywne emisje (fluorofory organiczne, białka fluorescencyjne, barwniki).
Główne elementy i zasada działania
- Źródło światła: lampy łukowe (rtęciowe, ksenonowe), diody LED oraz lasery — wybór zależy od potrzebnej mocy, stabilności i spektrum emisji.
- Filtry wzbudzające i emisyjne: separują promieniowanie wzbudzające od emitowanego; filtry emisyjne przepuszczają tylko światło fluorescencyjne określonego zakresu.
- Dichroiczny beamsplitter: odbija żywotne światło wzbudzające w kierunku próbki i jednocześnie przepuszcza światło fluorescencji do detektora — kluczowy element konstrukcji epifluorescencyjnej.
- Obiektyw: nie tylko powiększa, ale też dostarcza światło wzbudzające (epifluorescencja przez obiektyw), dlatego ważne są obiektywy o wysokiej aperturze numerycznej (NA) i dobrej transmisji dla odpowiednich długości fal.
- Detektor: okulary do obserwacji wzrokowej lub kamery (CCD, sCMOS) oraz przyrządy do pomiaru intensywności (fotopowielacze, PMT) — w mikroskopii konfokalnej używa się PMT.
Rodzaje mikroskopii fluorescencyjnej i usprawnienia
- Epifluorescencja — najczęstsza konstrukcja laboratoryjna, opisana powyżej.
- Konfokalna mikroskopia laserowa — wykorzystuje punktowe wzbudzanie laserem i szczelinę/pinhole do odcięcia światła poza płaszczyzną ogniskowania, co daje optyczne obrazowanie warstw (optyczna sekcja).
- Dwufotonowa mikroskopia — wzbudzanie za pomocą dwóch fotonów o dłuższych długościach fal (podczerwień), co zmniejsza fototoksyczność i pozwala na obrazowanie głębszych warstw tkanek.
- TIRF (Total Internal Reflection Fluorescence) — wykorzystuje pole ewanescentne do obrazowania zdarzeń przy powierzchni próbki (np. błona komórkowa) z bardzo dużym stosunkiem sygnału do tła.
- Super-rozdzielczość — techniki takie jak STED, PALM, STORM przekraczają klasyczny limit dyfrakcyjny (~200 nm) i umożliwiają obrazowanie struktur molekularnych z rozdzielczością rzędu dziesiątek nanometrów.
Typowe fluorofory i markery
Przykładowe fluorofory używane w praktyce: DAPI (barwi jądra), FITC, rhodamina, rodziny barwników Alexa, oraz białka fluorescencyjne jak GFP i jego mutacje. Wybór zależy od długości fali wzbudzającej/emisyjnej, jasności (kwantowego wydajności) i trwałości (odporności na fotobleaching).
Zastosowania
- Biologia komórkowa i molekularna: lokalizacja białek, obserwacja dynamiki komórek, badania sygnalizacji.
- Medycyna i diagnostyka: immunofluorescencja, testy jakościowe i ilościowe, patologia.
- Nauki o materiałach: badanie defektów, badania powierzchni i nanopowłok.
- Badania środowiskowe: oznaczanie zanieczyszczeń, algi i mikroorganizmy.
- Obrazowanie in vivo: badania małych zwierząt, wizualizacja procesów w tkankach.
- Zaawansowane techniki: FRET (badanie interakcji białek), FRAP (analiza mobilności molekularnej), single-molecule imaging.
Zalety i ograniczenia
- Zalety: wysoka czułość, specyficzność przy użyciu znakowanych przeciwciał/białek, możliwość obserwacji dynamicznych procesów i wielokolorowego obrazowania.
- Ograniczenia: fotobleaching (trwałe utraty sygnału przy naświetlaniu), fototoksyczność w badaniach żywych komórek, autofluorescencja tła, ograniczona rozdzielczość optyczna bez użycia metod super-rozdzielczości, konieczność odpowiedniego doboru fluoroforów i filtrów (przenikanie spektralne).
Przygotowanie próbki i dobre praktyki
- Wybierz fluorofory o odpowiednich spektrach oraz możliwie minimalnym nakładaniu się kanałów (unikaj zbytniego spektralnego overlap).
- Stosuj środki antyfade (np. DABCO, środki komercyjne) do mikroskopii obrazów długotrwałych i timelapse.
- Zadbaj o właściwe utrwalenie (dla obrazów stałych) lub warunki hodowli (dla live-cell), używaj mediów buforowych i kontroli temperatury/CO2 jeśli to konieczne.
- Minimalizuj ekspozycję światła wzbudzającego i intensywność źródła, aby zmniejszyć fotoksydację i photobleaching.
- Kalibruj system i stosuj odpowiednie znaczniki kontrolne (negatywne i pozytywne), aby rozróżnić sygnał specyficzny od tła.
Krótka lista praktycznych wskazówek
- Używaj obiektywów o wysokiej NA i odpowiedniej korekcji dla fluorescencji (np. plan-apochromat).
- Dobierz właściwe filtry i filtry emitujące dla używanych fluoroforów (kostki filtrów).
- Stosuj kamery o niskim szumie (sCMOS lub chłodzone CCD) do słabo emisyjnych próbek.
- Unikaj nadmiernego wzmacniania sygnału cyfrowego — lepsze jest dłuższe, ale kontrolowane napromienianie lub lepsze detektory.
- Dokumentuj ustawienia obrazowania (filtry, eksponowanie, wzmocnienie), aby wyniki były powtarzalne.
Mikroskopia fluorescencyjna jest wszechstronnym narzędziem badawczym, łączącym wysoką czułość z możliwością selektywnego znakowania struktur. Wybór konkretnej konfiguracji (epifluorescencja, konfokal, dwufotonowa, TIRF czy super-rozdzielczość) zależy od pytania badawczego, rodzaju próbki oraz wymogów dotyczących rozdzielczości i głębokości obrazowania.